Leave message
Can’t find what you’re looking for?
Fill out this form to inquire about our custom protein services!
Inquire about our Custom Services >>






























 Limited Edition Golden Llama is here! Check out how you can get one.
Limited Edition Golden Llama is here! Check out how you can get one.  Limited Edition Golden Llama is here! Check out how you can get one.
Limited Edition Golden Llama is here! Check out how you can get one.
 Offering SPR-BLI Services - Proteins provided for free!
Offering SPR-BLI Services - Proteins provided for free! Get your ComboX free sample to test now!
Get your ComboX free sample to test now!
 Time Limited Offer: Welcome Gift for New Customers !
Time Limited Offer: Welcome Gift for New Customers !  Shipping Price Reduction for EU Regions
Shipping Price Reduction for EU Regions
> Agonistische Zielproteine zur Beschleunigung der Entwicklung von Immuntherapien

Abgeleitet von der mit dem Nobelpreis ausgezeichneten Arbeit von Dr. James P. Allison und Dr. Tasuku Honjo wurden Immun-Checkpoint-Proteine als Schlüsselregulatoren des Immunsystems identifiziert. Die derzeit zugelassenen Medikamente sind jedoch Checkpoint-Inhibitoren. Das bedeutet, dass diese Medikamente verhindern sollen, dass ein „ABSCHALTEN“-Signal das Immunsystem erreicht. Aber was, wenn die Immunantwort einfach nicht ausreicht?
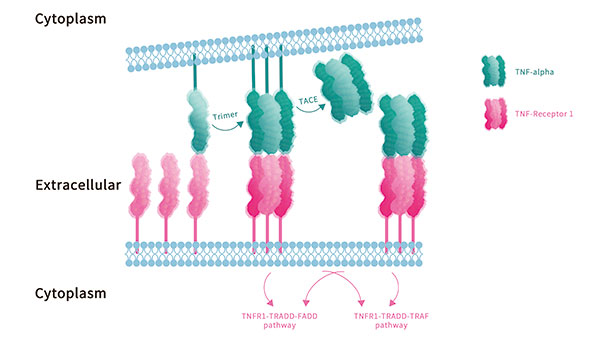
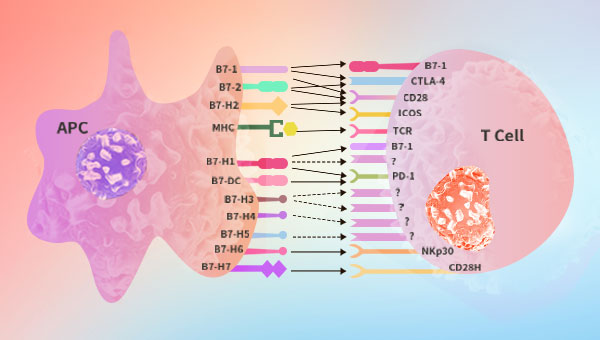
Agonisten, auch stimulierende Checkpoint-Moleküle genannt, sind dazu da, um „einen Gang zuzulegen“ oder Ihre Immunantwort zu beschleunigen. Anstatt das „ABSCHALTEN“-Signal zu hemmen, besteht der Schlüssel zu diesem Ziel darin, ständig grünes Licht zu geben, um die Immunantwort zu maximieren. Dies bedeutet, dass mehrere Kostimulatoren verwendet werden, um T-Zellen zu aktivieren. Beispielsweise ist die B7-CD28-Signalübertragung eine wichtige kostimulatorische Signalkaskade, die zur T-Zell-Aktivierung und Zytokinfreisetzung beiträgt. 4-1BB, OX40, Glucocorticoid-induzierter Tumor-Nekrose-Faktor (TNF)-Rezeptor (GITR) und andere Rezeptoren in der TNF-Superfamilie können mit der TCR-Signalgebung synergistisch wirken, um die T-Zell-Antworten und das Überleben zu verbessern. Agonisten kostimulatorischer Rezeptoren der Tumornekrosefaktor-Superfamilie (TNF-SF) und der B7-Familie erweisen sich daher als vielversprechende Optionen zur Erweiterung der immunmodulatorischen Toolbox.
ACROBiosystems hat eine Reihe von Produkten entwickelt, die auf kostimulierende Immunmoleküle der TNFSF Und B7-CD28-Familie abzielen, einschließlich Proteine, Überexpressionszelllinien und Inhibitor-Screening-Kits. Alle Produkte werden verifiziert und validiert, nicht nur als Endprodukte, sondern beginnend mit der Antikörperpräparation, dem ersten Screening, über die Produktion bis hin zur Qualitätskontrolle; Gewährleistung der besten Reagenzien und Werkzeuge zur Entwicklung Ihrer Agonisten-Immuntherapien.
Agonistische Zielproteine
Stabile Zelllinien
Testkits für Inhibitoren
| Molecule | Cat. No. | Description |
|---|---|---|
| OX40 Ligand | CHEK-ATP054 | HEK293/Human OX40 Ligand / TNFSF4 Stable Cell Line |
| OX40 | CHEK-ATP053 | HEK293/Human OX40 / TNFRSF4 / CD134 Stable Cell Line |
| 4-1BB Ligand | CHEK-ATP039 | HEK293/Human 4-1BB Ligand / TNFSF9 Stable Cell Line |
| 4-1BB | CHEK-ATP038 | HEK293/Human 4-1BB / TNFRSF9 Stable Cell Line |
![]() Strukturgenau mit hoher Reinheit, bestätigt durch SEC-MALS.
Strukturgenau mit hoher Reinheit, bestätigt durch SEC-MALS.
![]() Bestätigte Bindungsbioaktivität an Rezeptor oder Antikörper durch mehrere Technologieplattformen.
Bestätigte Bindungsbioaktivität an Rezeptor oder Antikörper durch mehrere Technologieplattformen.
![]() Verschiedene Speziesmarkierungen und Tags verfügbar, einschließlich Mensch, Maus, Ratte, Cynomolgus usw. für speziesübergreifende Studien.
Verschiedene Speziesmarkierungen und Tags verfügbar, einschließlich Mensch, Maus, Ratte, Cynomolgus usw. für speziesübergreifende Studien.
![]() Stabile Zelllinien für 4-1BB, OX40, etc. sind verfügbar!
Stabile Zelllinien für 4-1BB, OX40, etc. sind verfügbar!
![]() Inhibitor-Screening-Kits für CD27 usw. sind ebenfalls erhältlich!
Inhibitor-Screening-Kits für CD27 usw. sind ebenfalls erhältlich!
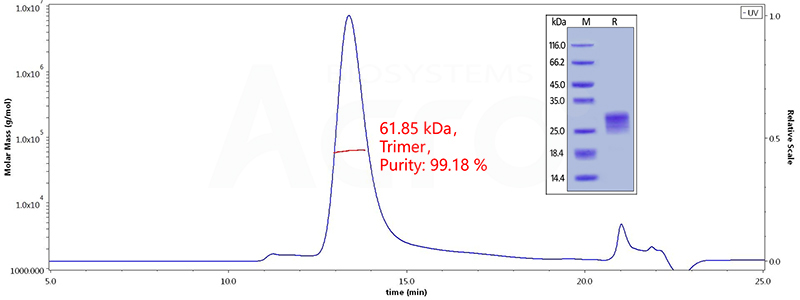
The purity of Human OX40 Ligand, His Tag (active trimer) (Cat. No. OXL-H52Q8 ) is more than 95% in HP-SEC, and the molecular weight of this protein is around 60-80 kDa verified by SEC-MALS.
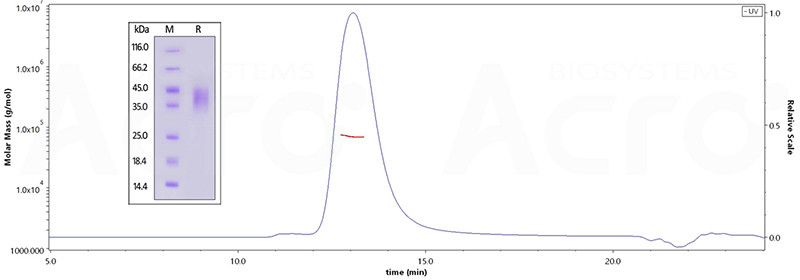
The purity of Human / Cynomolgus / Rhesus macaque CD28 Protein, His Tag (Cat. No. CD8-H52H3) is more than 90% and the molecular weight of this protein is around 65-75 kDa verified by SEC-MALS.
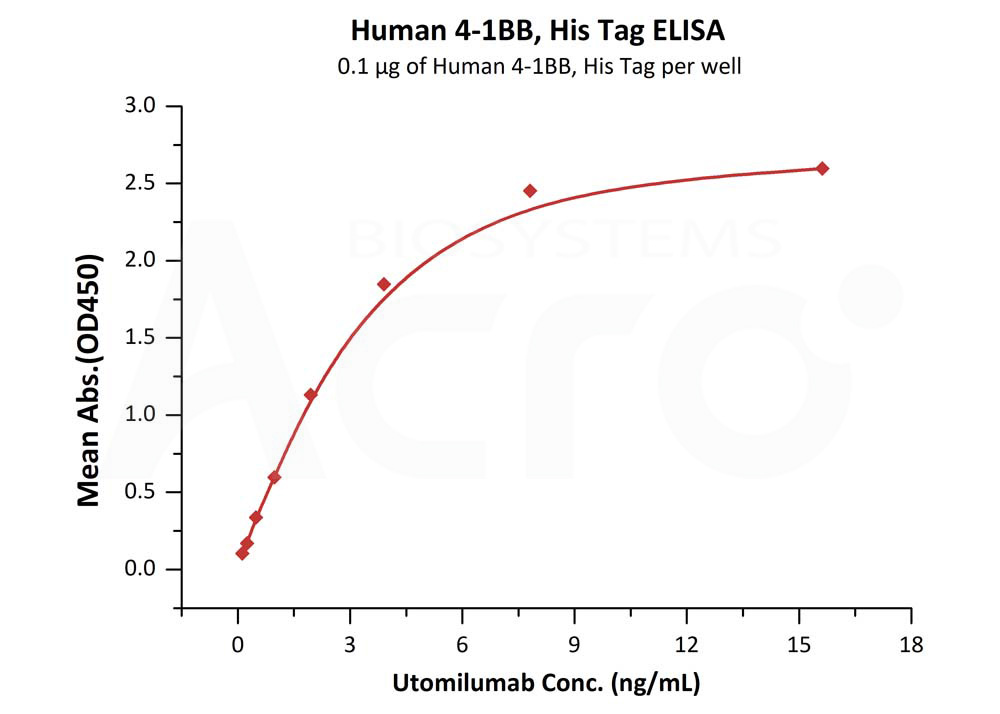
Immobilized Human 4-1BB, His Tag (Cat. No. 41B-H52Hc) at 1 μg/mL (100 μL/well) can bind Utomilumab with a linear range of 0.1-4 ng/mL (Routinely tested).
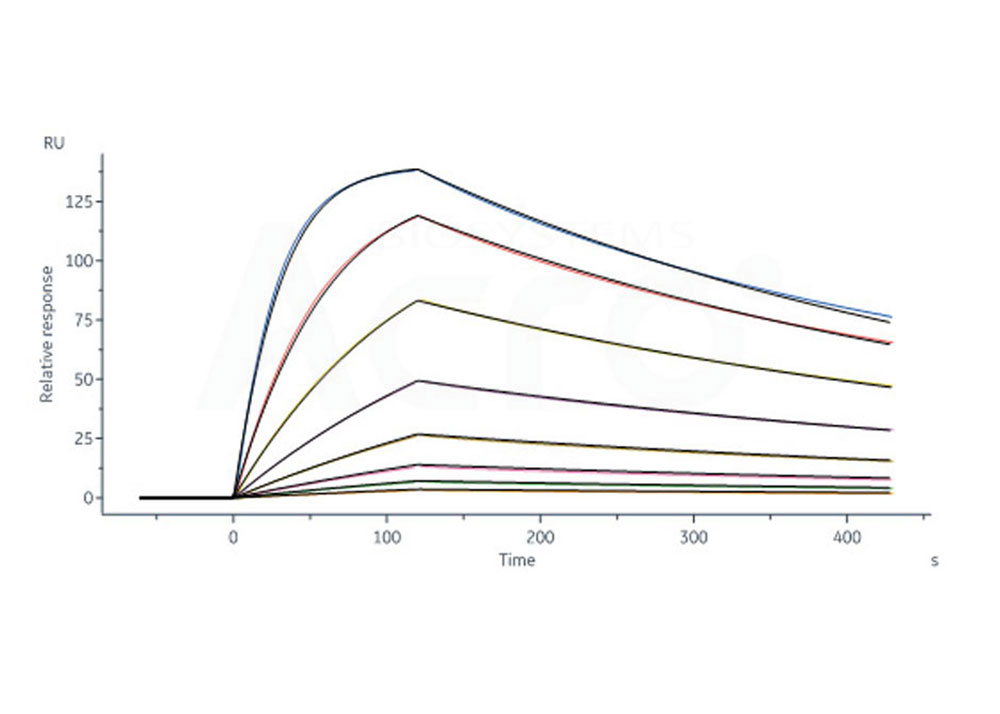
Human UreluMab captured on CM5 chip via Anti-human IgG Fc antibodies surface can bind Human 4-1BB, His Tag (Cat. No. 41B-H52Hc) with an affinity constant of 3.59 nM as determined in a SPR assay (Biacore 8K) (Routinely tested)
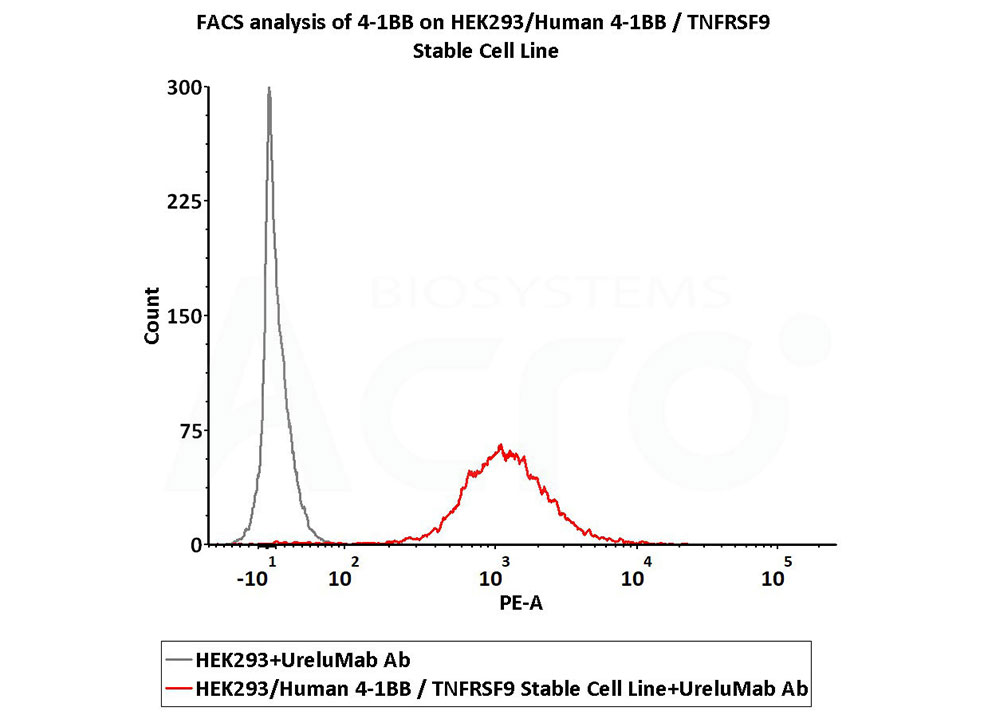
FACS assay shows that Monoclonal UreluMab antibody, Human IgG4 can bind to HEK293/Human 4-1BB / TNFRSF9 Stable Cell Line (CHEK-ATP038). HEK293/Human 4-1BB / TNFRSF9 Stable Cell Line was red line, Negative control HEK293 cells was grey line(QC tested).
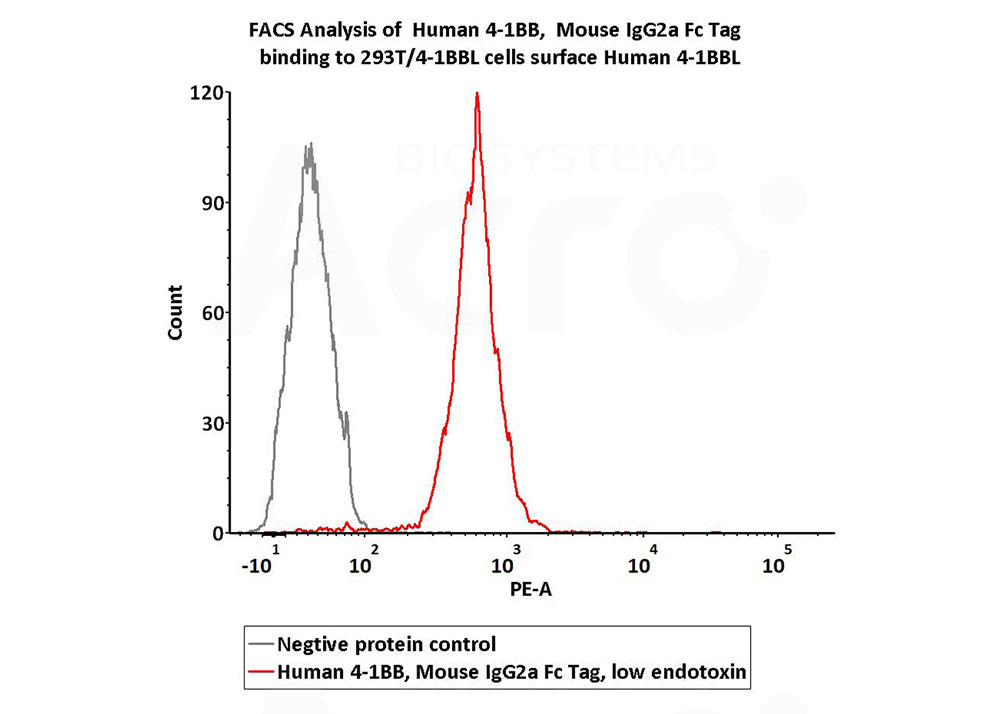
Flow Cytometry assay shows that Human 4-1BB Protein, Mouse IgG2a Fc Tag (Cat. No. 41B-H5256) can bind to 293T cells overexpressing Human 4-1BBL. The concentration of 4-1BB used is 0.03 μg/mL (Routinely tested).
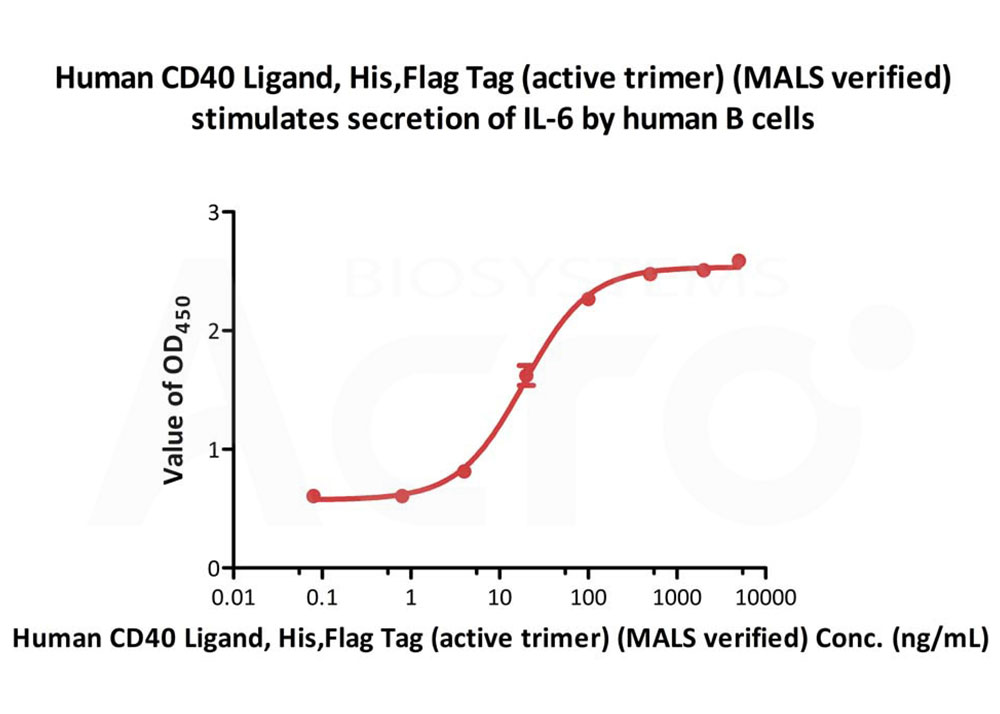
Human CD40 Ligand, His,Flag Tag (Cat. No. CDL-H52Db) stimulates secretion of IL-6 by human B cells. The ED50 for this effect is 18.76-19.45 ng/mL in the presence of 5 ng/mL of Recombinant Human IL 4 (Routinely tested).
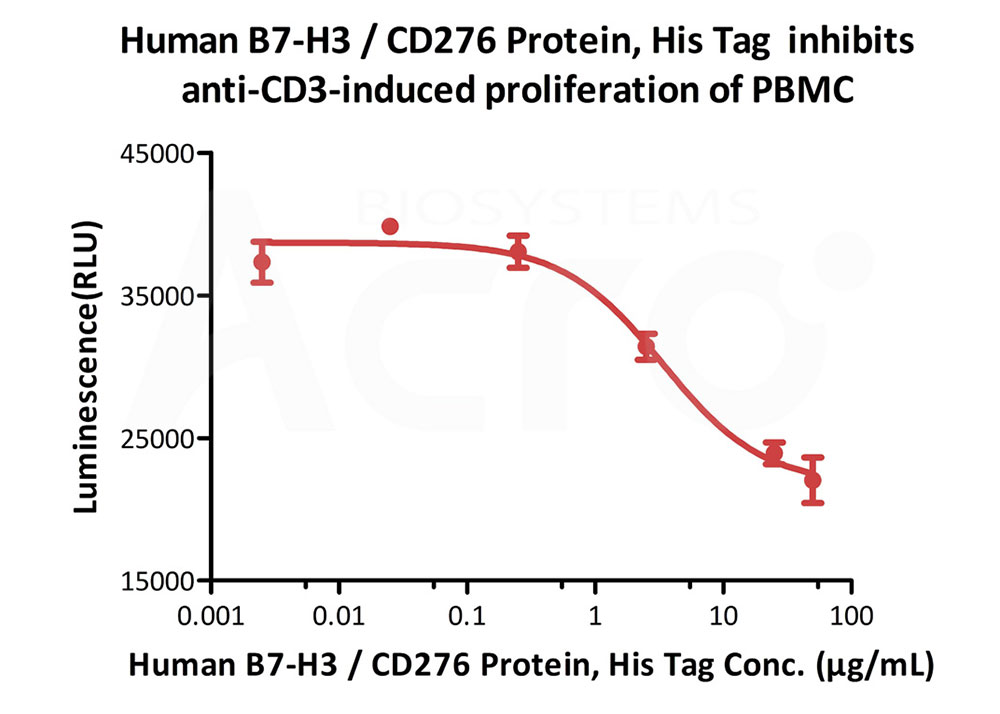
Human B7-H3, His Tag (Cat. No. B73-H52E2) inhibits Anti-CD3-induced proliferation of PBMC. The EC50 for this effect is 2.24-3.36 μg/mL (Routinely tested).
1. Choi Y, Shi Y, Haymaker CL, Naing A, Ciliberto G, Hajjar J. T-cell agonists in cancer immunotherapy. J Immunother Cancer. 2020 Oct;8(2):e000966. doi: 10.1136/jitc-2020-000966.
2. Elgueta R, Benson MJ, de Vries VC, et al.. Molecular mechanism and function of CD40/CD40L engagement in the immune system. Immunol Rev 2009;229:152–72.
This web search service is supported by Google Inc.